L’imaging rapido ha visto sviluppi sorprendenti negli ultimi anni, in particolare con l’avvento dei sensori digitali e la miniaturizzazione dei circuiti elettronici. Oggi esistono fotocamere ultraveloci in grado di rilevare fenomeni di estrema effimera. Abbiamo utilizzato una telecamera di questo tipo per esaminare i dettagli dei meccanismi in azione quando si svita una bottiglia di champagne.

Durante la presa di spuma (chiamata premio di spuma), il vino champagne produce anidride carbonica (CO2) – circa 5 litri per una bottiglia da 75 cl – che rimane intrappolata sotto pressione nella bottiglia chiusa. La pressione in una bottiglia ancora tappata varia molto con la sua temperatura. Così, a 20°C, la pressione raggiunge quasi 8 bar, che è 8 volte la pressione atmosferica, cioè la pressione che prevale a 70 metri sotto il livello del mare! La sequenza video nell’immagine sopra mostra i fenomeni che si verificano a seguito della fuoriuscita di un tappo da una bottiglia ad una pressione iniziale di 8 bar.
Quando il tappo esplode, il volume di anidride carbonica sotto pressione nel collo della bottiglia si espande improvvisamente. Quindi la sua pressione va da 8 bar ad una pressione ambiente di 1 bar. Questo è accompagnato da una diminuzione della sua temperatura: i fisici parlano di espansione adiabatica. Tuttavia, a seconda della sua temperatura e pressione, è probabile che una sostanza pura esista in tre fasi: gassosa, liquida e solida. Pertanto, a una pressione di 1 bar, l’acqua diventa liquida a 20 ° C, si trasforma in ghiaccio al di sotto di 0 ° C e bolle in vapore a 100 ° C. Ma per quanto riguarda l’anidride carbonica? Alla pressione di 1 bar, l’anidride carbonica rimane allo stato gassoso al di sopra di una temperatura di -78,5°C; Al di sotto di questa temperatura critica, esiste nella sua forma solida: ghiaccio secco.
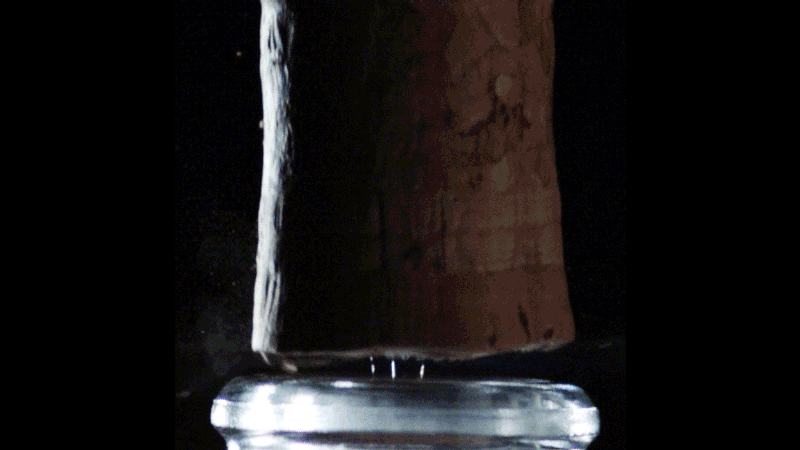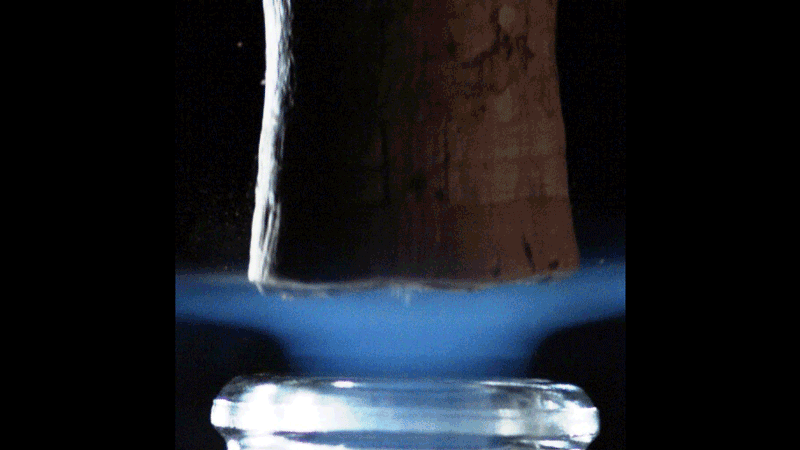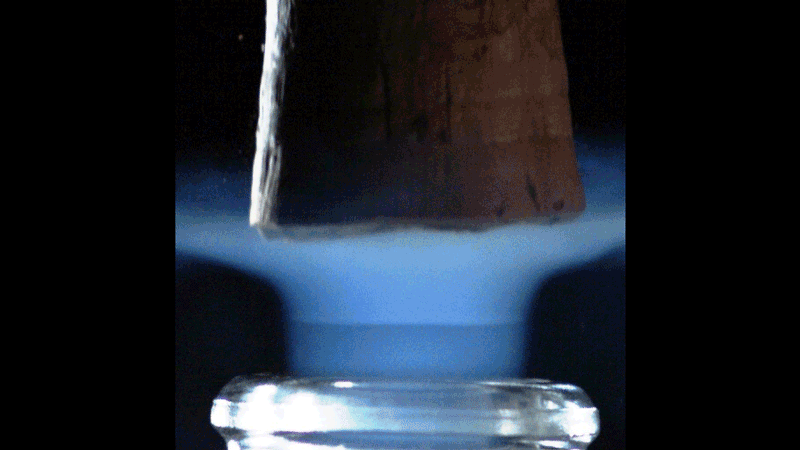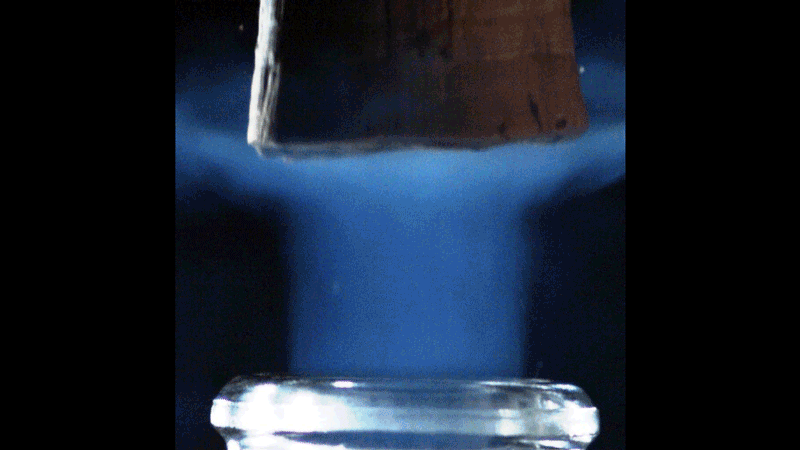
Durante lo sblocco, ghiaccio secco e onde d’urto
Per questa bottiglia ad una pressione iniziale di 8 bar, la temperatura dell’anidride carbonica in espansione scende improvvisamente a circa -90°C. Quindi vengono convertiti i fumi di anidride carbonica Piccoli cristalli di ghiaccio seccoCapace di diffondere la luce ambientale. Il colore azzurro del pennacchio è un segno delle dimensioni molto ridotte di questi cristalli. Infatti, particelle o particelle più piccole delle lunghezze d’onda dello spettro luminoso ambiente (centrato intorno a 0,6 micrometri) disperdono più efficacemente le piccole lunghezze d’onda dello spettro (il blu, in particolare) rispetto alle lunghezze d’onda maggiori (come il rosso): questo è chiamato dispersione di Rayleigh. È lo stesso fenomeno che spiega perché il cielo ci appare blu: le molecole che compongono l’atmosfera del nostro pianeta sono molto più piccole delle lunghezze d’onda della luce solare, quindi il colore blu è disperso in modo più efficiente rispetto ad altri colori dello spettro.
Hai notato la piccola linea orizzontale che interseca la colonna blu? Di onda d’urto Una caratteristica degli aerei supersonici, noti come dischi di Mach. Appare circa 500 μs dopo lo sblocco e progredisce sulla scia del blocco prima di svanire dopo circa 500 μs. Onde d’urto simili si trovano nel pennacchio supersonico espulso dai reattori di un jet da combattimento o di un missile. Durante il primo millisecondo dopo l’espulsione del tappo, il collo della bottiglia di champagne si comporta in qualche modo come l’ugello di un reattore a razzo. Chi ci avrebbe creduto!
Questa analisi è stata scritta da Gerard Leger-Beller, Professore di Fisica nel Laboratorio di Enologia dell’Università di Reims-Champaign-Ardennes (URCA).
L’articolo originale è stato pubblicato su Conversazione.


“Appassionato di alcol. Piantagrane. Introverso. Studente. Amante dei social media. Ninja del web. Fan del bacon. Lettore”.


